KYPROLIS
Estás aquí
Contáctanos
¿Para qué sirve el medicamento Kyprolis?
Útil en el tratamiento del mieloma múltiple en recaída o refractario.
¿Cómo se aplica el medicamento Kyprolis?
En pacientes con superficie corporal mayor a 22 m2, calcular la dosis con base a un área de superficie corporal de 22 m2.
¿Qué contiene el medicamento Kyprolis?
Carfilzomib.

Kyprolis es un polvo liofilizado blanco estéril para solución para inyección/mediante infusión.
El frasco ámpula con polvo liofilizado contiene:
Carfilzomib ............. 60 mg
Excipiente ............... cbp.
Mieloma Múltiple en Recaída o Refractario
Kyprolis está indicado para el tratamiento de pacientes adultos con mieloma múltiple en recaída o refractario que han recibido de una a tres líneas de terapia en combinación con:
- lenalidomida y dexametasona; o
- dexametasona; o
- daratumumab y dexametasona.
Kyprolis está indicado como agente único para el tratamiento de pacientes adultos con mieloma múltiple en recaída o refractario, y que hayan recibido una o más líneas de terapia.
Kyprolis está contraindicado en pacientes con hipersensibilidad a carfilzomib o sus derivados, o cualquier excipiente en la formulación.
Las siguientes reacciones adversas se discuten con mayor detalle en la sección Precauciones Generales de la información para prescribir:
- Toxicidades Cardiacas
- Falla Renal Aguda
- Síndrome de Lisis Tumoral
- Toxicidad Pulmonar
- Hipertensión Pulmonar
- Disnea
- Hipertensión
- Trombosis Venosa
- Reacciones Relacionadas a la Infusión
- Hemorragia
- Trombocitopenia
- Toxicidad Hepática y Falla Hepática
- Microangiopatía Trombótica
- Síndrome de Encefalopatía Posterior Reversible.
- Leucoencefalopatía Multifocal Progresiva.
Experiencia de Estudios Clínicos
Dado que los estudios clínicos son conducidos bajo condiciones ampliamente variables, los índices de eventos adversos observados en los estudios clínicos de un fármaco no pueden ser directamente comparados con índices en los estudios clínicos de otro fármaco y pueden no reflejar los índices observados en la práctica médica.
La población de seguridad agrupada descrita en Precauciones generales refleja la exposición a Kyprolis en 1789 pacientes, administrado en combinación con otros medicamentos en ASPIRE, ENDEAVOR, A.R.R.O.W. y CANDOR. Las reacciones adversas más comunes que se produjeron en al menos un 20% de los pacientes que recibieron Kyprolis combinado con otros fármacos fueron anemia, diarrea, fatiga, hipertensión, pirexia, infección del tracto respiratorio superior, trombocitopenia, tos, disnea e insomnio.
Kyprolis en Combinación con Lenalidomida y Dexametasona
La seguridad de Kyprolis 20/27 mg/m2 dos veces a la semana en combinacionón con lenalidomida y dexametasona (KRd) fue evaluada en ASPIRE (ver Estudios clínicos). La mediana del número de ciclos iniciados fue 22 ciclos para el brazo KRd y 14 ciclos para el brazo Rd.
Ocurrieron muertes debidas a reacciones adversas dentro de los 30 días desde la última dosis de cualquier terapia en el brazo KRd en 45/392 (12%) pacientes comparado con 42/389 (11%) pacientes que murieron debido a eventos adversos dentro de los 30 días desde la última dosis de cualquier terapia Rd. La causa más común de muerte en pacientes (%) en los dos brazos (KRd versus Rd) incluyó infección 12 (3%) versus 11 (3%), cardiaca 10 (3%) versus 9 (2%), y otras reacciones adversas 23 (6%) versus 22 (6%). Se reportaron reacciones adversas graves en 65% de los pacientes en el brazo de KRd y 57% de los pacientes en el brazo de Rd. Las reacciones adversas graves más comunes reportadas en el brazo de KRd en comparación con el brazo de Rd fueron neumonía (17% versus 13%), infección del tracto respiratorio (4% versus 2%), pirexia (4% versus 3%), y embolismo pulmonar (3% versus 2%). En los pacientes tratados con Kyprolis, el 47% tenía 65 años o más y el 11% tenía 75 años o más. La incidencia de eventos adversos graves fue del 57% en pacientes menores de 65 años, 73% en pacientes de 65 a 74 años y 81% en pacientes ≥ 75 años [ver Precauciones generales (toxicidad cardíaca) y uso en Poblaciones específicas (Uso Geriátrico)]. La interrupción debida a cualquier reacción adversa ocurrió en el 33% en el brazo KRd versus el 30% en el brazo Rd. Las reacciones adversas que llevaron a la interrupción de Kyprolis ocurrieron en el 12% de los pacientes y las reacciones más comunes incluyeron neumonía (1%), infarto de miocardio (0.8%) e infección del tracto respiratorio superior (0.8%). La incidencia de eventos de insuficiencia cardíaca fue del 7% en el brazo KRd versus el 4% en el brazo Rd.
La Tabla 17 resume las reacciones adversas en los primeros 12 ciclos en ASPIRE.
Tabla 17: Reacciones Adversas Más Comunes que Ocurrieron en los Ciclos 1 a 12 (≥ 10%) en Pacientes que Recibieron KRd (Régimen de 20/27 mg/m2) en ASPIRE
|
Reacciones Adversas |
KRd |
Rd |
||
|---|---|---|---|---|
|
Cualquier Grado |
Grado ≥3 |
Cualquier Grado |
Grado ≥3 |
|
|
Trastornos de la Sangre y del Sistema Linfático |
||||
|
Anemia |
138 (35) |
53 (14) |
127 (33) |
47 (12) |
|
Neutropenia |
124 (32) |
104 (27) |
115 (30) |
89 (23) |
|
Trombocitopenia |
100 (26) |
58 (15) |
75 (19) |
39 (10) |
|
Trastornos Gastrointestinales |
||||
|
Diarrea |
119 (30) |
8 (2) |
106 (27) |
12 (3) |
|
Estreñimiento |
68 (17) |
0 (0) |
55 (14) |
1 (0) |
|
Náusea |
63 (16) |
1 (0) |
43 (11) |
3 (1) |
|
Trastornos Generales y Alteraciones en el Lugar de Administración |
||||
|
Fatiga |
113 (29) |
23 (6) |
107 (28) |
20 (5) |
|
Pirexia |
93 (24) |
5 (1) |
64 (17) |
1 (0) |
|
Edema periférico |
59 (15) |
3 (1) |
48 (12) |
2 (1) |
|
Astenia |
54 (14) |
11 (3) |
49 (13) |
7 (2) |
|
Infecciones |
||||
|
Infección del tracto respiratorio superior |
87 (22) |
7 (2) |
54 (14) |
4 (1) |
|
Bronquitis |
55 (14) |
5 (1) |
40 (10) |
2 (1) |
|
Infección viral del tracto respiratorio superior |
55 (14) |
0 (0) |
44 (11) |
0 (0) |
|
Neumoníaa |
54 (14) |
35 (9) |
43 (11) |
27 (7) |
|
Trastornos del Metabolismo y de la Nutrición |
||||
|
Hipocalemia |
78 (20) |
22 (6) |
35 (9) |
12 (3) |
|
Hipocalcemia |
55 (14) |
10 (3) |
39 (10) |
5 (1) |
|
Hiperglucemia |
43 (11) |
18 (5) |
33 (9) |
15 (4) |
|
Trastornos Musculoesqueléticos y del Tejido Conjuntivo |
||||
|
Espasmos musculares |
92 (24) |
3 (1) |
75 (19) |
3 (1) |
|
Dolor de Espalda |
41 (11) |
4 (1) |
54 (14) |
6 (2) |
|
Trastornos del Sistema Nervioso |
||||
|
Neuropatías periféricasb |
43 (11) |
7 (2) |
39 (10) |
4 (1) |
|
Trastornos Psiquiátricos |
||||
|
Insomnio |
64 (16) |
6 (2) |
51 (13) |
8 (2) |
|
Trastornos Respiratorios, Torácicos, y Mediastínicos |
||||
|
Tosc |
93 (24) |
2 (1) |
54 (14) |
0 (0) |
|
Disnead |
71 (18) |
8 (2) |
61 (16) |
6 (2) |
|
Trastornos de la Piel y del Tejido Subcutáneo |
||||
|
Erupción |
45 (12) |
5 (1) |
54 (14) |
5 (1) |
|
Trastornos Vasculares |
||||
|
Eventos trombóticos y embólicose |
49 (13) |
16 (4) |
23 (6) |
9 (2) |
|
Hipertensiónf |
41 (11) |
12 (3) |
15 (4) |
4 (1) |
KRd = Kyprolis, lenalidomida, y dexametasona; Rd = lenalidomida y dexametasona
a Neumonía incluye neumonía y bronconeumonía.
b Neuropatías periféricas incluye neuropatía periférica, neuropatía periférica sensorial, y neuropatía periférica motora.
c Tos incluye tos y tos productiva.
d Disnea incluye disnea y disnea por esfuerzo.
e Eventos venosos trombóticos y embólicos, incluyen trombosis venosa profunda, embolismo pulmonar, tromboflebitis superficial, tromboflebitis, trombosis venosa de extremidad, síndrome post-trombótico, trombosis venosa.
f Hipertensión incluye hipertensión, crisis hipertensiva.
Hubo 274 (70%) pacientes en el brazo KRd que recibieron tratamiento más allá del Ciclo 12. No hubo nuevas reacciones adversas clínicamente relevantes que emergieran en los ciclos de tratamiento posteriores.
Reacciones Adversas que ocurren a una Frecuencia de < 10%
- Trastornos de la sangre y del sistema linfático: neutropenia febril, linfopenia.
- Trastornos cardiacos: paro cardiaco, insuficiencia cardiaca, insuficiencia cardiaca congestiva, infarto al miocardio, isquemia de miocardio, efusión pericárdica.
- Trastornos del oído y laberínticos: sordera, tinnitus
- Trastornos oculares: catarata, visión borrosa.
- Trastornos gastrointestinales: dolor abdominal, dolor abdominal superior, dispepsia, hemorragia gastrointestinal, dolor de muelas.
- Trastornos generales y alteraciones en el lugar de administración: escalofríos, reacción en el sitio de infusión, falla orgánica múltiple, dolor.
- Infecciones: colitis por clostridium difficiele, influenza, infección pulmonar, rinitis, septicemia, infección del tracto urinario, infección viral.
- Trastornos del metabolismo y de la nutrición: deshidratación, hipercalemia, hiperuricemia, hipoalbuminemia, hiponatremia, síndrome de lisis tumoral.
- Trastornos musculoesqueléticos y del tejido conjuntivo: debilidad muscular, mialgia.
- Trastornos del sistema nervioso: hipoestesia, hemorragia intracraneal, parestesia.
- Trastornos psiquiátricos: ansiedad, delirio.
- Trastornos renales y urinarios: insuficiencia renal, insuficiencia renal aguda, daño renal.
- Trastornos respiratorios, torácicos y mediastínicos: disfonía, epistaxis, dolor orofaríngeo, embolismo pulmonar, edema pulmonar, hemorragia pulmonar.
- Trastornos de la piel y del tejido subcutáneo: eritema, hiperhidrosis, prurito.
- Trastornos vasculares: trombosis de vena profunda, hemorragia, hipotensión.
Las reacciones adversas Grado 3 o mayor que ocurrieron durante los Ciclos 1 a 12 con una diferencia sustancial (≥ 2%) entre los dos brazos fueron neutropenia, trombocitopenia, hipocalemia e hipofosfatemia.
La Tabla 18 describe las anormalidades de laboratorio Grado 3 a 4 reportadas en ASPIRE.
Tabla 18: Anormalidades de Laboratorio Grado 3 a 4 (≥ 10%) durante los Ciclos 1 a 12 en Pacientes que Recibieron KRd (Régimen de 20/27 mg/m2) en ASPIRE
|
Anormalidad de Laboratorio |
KRd |
Rd |
|---|---|---|
|
Disminución de linfocitos |
182 (46) |
119 (31) |
|
Disminución de la cuenta absoluta de neutrófilos |
152 (39) |
141 (36) |
|
Disminución de fósforo |
122 (31) |
106 (27) |
|
Disminución de plaquetas |
101 (26) |
59 (15) |
|
Disminución de la cuenta total de glóbulos blancos |
97 (25) |
71 (18) |
|
Disminución de hemoglobina |
58 (15) |
68 (18) |
|
Aumento de glucosa |
53 (14) |
30 (8) |
|
Disminución de potasio |
41 (11) |
23 (6) |
KRd = Kyprolis, lenalidomida, y dexametasona; Rd = lenalidomida y dexametasona
Kyprolis en Combinación con Dexametasona
La seguridad de Kyprolis en combinación con dexametasona fue evaluada en dos estudios abiertos, aleatorizados (ENDEAVOR y A.R.R.O.W.) (ver Estudios Clínicos).
ENDEAVOR
La seguridad de Kyprolis 20/56 mg/m2 dos veces a la semana en combinación con dexametasona (Kd) se evaluó en ENDEAVOR (ver Estudios Clínicos). Los pacientes recibieron tratamiento durante una mediana de 48 semanas en el grupo de Kd y 27 semanas en el brazo de bortezomib/dexametasona (Vd).
Ocurrieron muertes debidas a reacciones adversas dentro de los 30 días del último tratamiento de estudio en 32/463 (7%) pacientes en el brazo de Kd y 21/456 (5%) pacientes en el brazo de Vd. Las causas de muerte que ocurrieron en pacientes (%) en los dos brazos (Kd versus Vd) incluyeron cardiaca 4 (1%) versus 5 (1%), infecciones 8 (2%) versus 8 (2%), progresión de la enfermedad 7 (2%) versus 4 (1%), pulmonar 3 (1%) versus 2 (< 1%), renal 1 (< 1%) versus 0 (0%), y otros eventos adversos 9 (2%) versus 2 (< 1%).
Se reportaron reacciones adversas graves en 59% de los pacientes en el brazo de Kd y 40% de los pacientes en el brazo de Vd.En ambos brazos de tratamiento, la neumonía fue la reacción adversa grave más comúnmente reportada (8% versus 9%). Entre los pacientes tratados con Kyprolis, el 52% tenía 65 años o más y el 17% tenía 75 y más. La incidencia de eventos adversos graves fue del 54% en pacientes menores de 65 años, 60% en pacientes de 65 a 74 años y 69% en pacientes ≥ 75 años [ver Precauciones generales y Uso en poblaciones específicas (uso Geriátrico)]. La descontinuación debida a cualquier reacción adversa ocurrió en 29% en el brazo de Kd versus 26% en el brazo de Vd. La reacción más común que llevó a la descontinuación fue insuficiencia cardiaca en el brazo de Kd (n = 8, 2%) y neuropatía periférica en el brazo de Vd (n = 22, 5%). La incidencia de eventos de falla cardiaca fue de 11% en el brazo Kd versus 3% en el brazo Vd.
Las reacciones adversas en los primeros 6 meses de la terapia que ocurrieron en una tasa de 10% o más en el brazo Kd se presentan en la Tabla 19.
Tabla 19: Reacciones Adversas Más Comunes (≥ 10%) Ocurriendo en los Meses 1 a 6 en Pacientes que Recibieron Kd (Régimen de 20/56 mg/m2) en ENDEAVOR
|
Reacción Adversa |
Kd |
Vd |
|||
|---|---|---|---|---|---|
|
Cualquier Grado |
Grado ≥3 |
Cualquier Grado |
Grado ≥3 |
||
|
Trastornos de la Sangre y del Sistema Linfático |
|||||
|
Anemia |
161 (35) |
57 (12) |
112 (25) |
43 (9) |
|
|
Trombocitopeniaa |
125 (27) |
45 (10) |
112 (25) |
64 (14) |
|
|
Trastornos Gastrointestinales |
|||||
|
Diarrea |
117 (25) |
14 (3) |
149 (33) |
27 (6) |
|
|
Náusea |
70 (15) |
4 (1) |
68 (15) |
3 (1) |
|
|
Constipación |
60 (13) |
1 (0) |
113 (25) |
6 (1) |
|
|
Vómito |
45 (10) |
5 (1) |
33 (7) |
3 (1) |
|
|
Trastornos Generales y Alteraciones en el Lugar de Administración |
|||||
|
Fatiga |
116 (25) |
14 (3) |
126 (28) |
25 (6) |
|
|
Pirexia |
102 (22) |
9 (2) |
52 (11) |
3 (1) |
|
|
Astenia |
73 (16) |
9 (2) |
65 (14) |
13 (3) |
|
|
Edema periférico |
62 (13) |
3 (1) |
62 (14) |
3 (1) |
|
|
Infecciones |
|||||
|
Infección del tracto respiratorio superior |
67 (15) |
4 (1) |
55 (12) |
3 (1) |
|
|
Bronquitis |
54 (12) |
5 (1) |
25 (6) |
2 (0) |
|
|
Trastornos Musculoesqueléticos y del Tejido Conjuntivo |
|||||
|
Espasmos musculares |
70 (15) |
1 (0) |
23 (5) |
3 (1) |
|
|
Dolor de espalda |
64 (14) |
8 (2) |
61 (13) |
10 (2) |
|
|
Trastornos del Sistema Nervioso |
|||||
|
Dolor de cabeza |
67 (15) |
4 (1) |
39 (9) |
2 (0) |
|
|
Neuropatías periféricasb,c |
56 (12) |
7 (2) |
170 (37) |
23 (5) |
|
|
Trastornos Psiquiátricos |
|||||
|
Insomnio |
105 (23) |
5 (1) |
116 (25) |
10 (2) |
|
|
Trastornos Respiratorios, Torácicos, y Mediastínicos |
|||||
|
Disnead |
128 (28) |
23 (5) |
69 (15) |
8 (2) |
|
|
Tose |
97 (21) |
0 (0) |
61 (13) |
2 (0) |
|
|
Trastornos Vasculares |
|||||
|
Hipertensiónf |
83 (18) |
30 (7) |
33 (7) |
12 (3) |
|
Kd = Kyprolis y dexametasona; Vd = bortezomib y dexametasona
a La trombocitopenia incluye disminución de cuenta de plaquetas y trombocitopenia.
b Neuropatías periféricas incluyen neuropatía periférica, neuropatía periférica sensorial, neuropatía periférica motora.
c Ver Estudios Clínicos, En combinación con dexametasona para el tratamiento de pacientes con mieloma múltiple en recaída o refractaria.
d Disnea incluye disnea y disnea por esfuerzo.
e Tos incluye tos y tos productiva.
f Hipertensión incluye hipertensión, crisis hipertensiva, y emergencia hipertensiva.
La tasa de evento de neuropatía periférica ≥ Grado 2 en el brazo de Kd fue de7% (IC 95%: 5, 9) versus 35% (IC 95%: 31, 39) en el brazo Vd.
Reacciones Adversas que Ocurrena una Frecuencia de < 10%
- Trastornos de la sangre y del sistema linfático: neutropenia febril, leucopenia, linfopenia, neutropenia, microangiopatía trombótica, púrpura trombocitopénica trombótica.
- Trastornos cardiacos: fibrilación atrial, paro cardiaco, falla cardiaca, insuficiencia cardiaca congestiva, infarto al miocardio, isquemia de miocardio, palpitaciones, taquicardia.
- Trastornos del oído y laberínticos: tinnitus
- Trastornos oculares: catarata, visión borrosa.
- Trastornos gastrointestinales: dolor abdominal, dolor abdominal superior, dispepsia, hemorragia gastrointestinal, dolor de muelas.
- Trastornos generales y alteraciones en el sitio de administración: dolor de pecho, escalofríos, enfermedad parecida a la influenza, reacciones en el sitio de infusión (incluyendo inflamación, dolor, y eritema), malestar, dolor.
- Trastornos hepatobiliares: colestasis, insuficiencia hepática, hiperbilirrubinemia.
- Trastornos del sistema inmune: hipersensibilidad al fármaco.
- Infecciones: bronconeumonía, gastroenteritis, influenza, infección pulmonar, nasofaringitis, neumonía, rinitis, septicemia, infección del tracto urinario, infección viral.
- Trastornos del metabolismo y de la nutrición: disminución de apetito, deshidratación, hipercalcemia, hipercalemia, hiperuricemia, hipoalbuminemia, hipocalcemia, hipomagnesemia, hiponatremia, hipofosfatemia, síndrome de lisis tumoral.
- Trastornos musculoesqueléticos y del tejido conjuntivo: debilidad muscular, dolor musculoesquelético de pecho, dolor musculoesquelético, mialgia.
- Trastornos del sistema nervioso: accidente cerebrovascular, mareo, hipoestesia, parestesia, síndrome de encefalopatía posterior reversible.
- Trastornos psiquiátricos: ansiedad.
- Trastornos renales y urinarios: insuficiencia renal, insuficiencia renal aguda, daño renal.
- Trastornos respiratorios, torácicos, y mediastínicos: síndrome de dificultad respiratoria aguda, disfonía, epistaxis, enfermedad pulmonar intersticial, dolor orofaríngeo, neumonitis, embolismo pulmonar, edema pulmonar, hipertensión pulmonar, sibilancias.
- Trastornos de la piel y del tejido subcutáneo: eritema, hiperhidrosis, prurito, erupciones.
- Trastornos vasculares: trombosis venosa profunda, enrojecimiento, hipotensión.
La Tabla 20 describe anormalidades de laboratorio Grado 3 a 4 reportadas en una tasa de ≥ 10% en el brazo Kd.
Tabla 20: Anormalidades de Laboratorio Grado 3 a 4 (≥ 10%) en los Meses 1 a 6 en Pacientes que recibieron Kd (Régimen de 20/56 mg/m2) en ENDEAVOR
|
Anormalidad de Laboratorio |
Kd |
Vd |
|---|---|---|
|
Disminución de linfocitos |
249 (54) |
180 (40) |
|
Incremento del ácido úrico |
244 (53) |
198 (43) |
|
Disminución de hemoglobina |
79 (17) |
68 (15) |
|
Disminución de plaquetas |
85 (18) |
77 (17) |
|
Disminución de fósforo |
74 (16) |
61 (13) |
|
Disminución en la depuración de creatininaa |
65 (14) |
49 (11) |
|
Incremento de potasio |
55 (12) |
21 (5) |
Kd = Kyprolis y dexametasona; Vd = bortezomib y dexametasona
a Calculado usando la fórmula de Cockcroft-Gault.
A.R.R.O.W.
La seguridad de Kyprolis en combinación con dexametasona se evaluó en A.R.R.O.W. (ver Estudios Clínicos). Los pacientes de A.R.R.O.W. recibieron tratamiento durante una mediana de 38 semanas en el brazo de Kd 20/70 mg/m2 una vez a la semana y de 29,1 semanas en el brazo de Kd 20/27 mg/m2 dos veces por semana. El perfil de seguridad para el régimen de Kd 20/70 mg/m2 una vez a la semana fue similar al de Kd 20/27 mg/m2 dos veces a la semana.
Las muertes debidas a reacciones adversas dentro de los 30 días posteriores al último tratamiento del estudio ocurrieron en 22/238 (9%) pacientes en el brazo de Kd 20/70 mg/m2 y en 18/235 (8%) pacientes en el brazo Kd 20/27 mg/m2. Las reacciones adversas fatales más frecuentes que ocurren en pacientes (%) en los dos brazos (una vez por semana Kd 20/70 mg/m2 versus dos veces por semana Kd 20/27 mg/m2) fueron sepsis 2 (<1%) versus 2 (<1 %), shock séptico 2 (<1%) versus 1 (<1%) e infección 2 (<1%) versus 0 (0%).
Se notificaron reacciones adversas graves en el 43% de los pacientes en el brazo de Kd 20/70 mg/m2 y en el 41% de los pacientes en el brazo de Kd 20/27 mg/m2. En ambos grupos de tratamiento, la neumonía fue la reacción adversa grave más frecuentemente reportada (8% versus 7%).
La interrupción debida a cualquier reacción adversa ocurrió en el 13% en el brazo de Kd 20/70 mg/m2 frente al 12% en el brazo de Kd 20/27 mg/m2. La reacción más común que llevó a la interrupción fue la lesión renal aguda (2% versus 2%). La incidencia de eventos de falla cardíaca fue del 3.8% en el brazo de Kd 20/70 mg/m2 una vez a la semana versus el 5.1% en el brazo de Kd 20/27 mg/m2 dos veces a la semana.
Las reacciones adversas que ocurrieron a una tasa del 10% o más en cualquiera de los brazos Kd se presentan en la Tabla 21.
Tabla 21: Reacciones adversas en Pacientes que Recibieron Kd (≥ 10% en cualquier brazo Kd) en A.R.R.O.W.
|
Reacción Adversa |
Una vez por semana Kd 20/70 mg/m2 |
Dos veces por semana Kd 20/27 mg/m2 |
|||
|
Cualquier grado |
Grado ≥3 |
Cualquier grado |
Grado ≥3 |
||
|
Trastornos de la Sangre y del Sistema Linfático |
|||||
|
Anemiaa |
64 (26.9) |
42 (17.6) |
76 (32.3) |
42 (17.9) |
|
|
Trombocitopeniab |
53 (22.3) |
26 (10.9) |
41 (17.4) |
27 (11.5) |
|
|
Neutropeniac |
30 (12.6) |
21 (8.8) |
27 (11.5) |
17 (7.2) |
|
|
Transtornos Gastrointestinales |
|||||
|
Diarrea |
44 (18.5) |
2 (0.8) |
47 (20.0) |
3 (1.3) |
|
|
Náusea |
34 (14.3) |
1 (0.4) |
26 (11.1) |
2 (0.9) |
|
|
Transtornos Generales y Alteraciones en el Lugar de Administración |
|||||
|
Pirexia |
55 (23.1) |
2 (0.8) |
38 (16.2) |
4 (1.7) |
|
|
Fatiga |
48 (20.2) |
11 (4.6) |
47 (20.0) |
5 (2.1) |
|
|
Astenia |
24 (10.1) |
3 (1.3) |
25 (10.6) |
2 (0.9) |
|
|
Edema periférico |
18 (7.6) |
0 (0.0) |
25 (10.6) |
2 (0.9) |
|
|
Infecciones |
|||||
|
Infección del tracto respiratoriod |
70 (29.4) |
7 (2.9) |
79 (33.6) |
7 (3.0) |
|
|
Neumonia |
28 (11.8) |
24 (10.1) |
20 (8.5) |
16 (6.8) |
|
|
Bronquitis |
27 (11.3) |
2 (0.8) |
25 (10.6) |
5 (2.1) |
|
|
Trastornos musculoesqueléticos y del Tejido Conjuntivo |
|||||
|
Dolor de espalda |
28 (11.8) |
2 (0.8) |
28 (11.9) |
4 (1.7) |
|
|
Transtornos del Sistema Nervioso |
|||||
|
Dolor de cabeza |
25 (10.5) |
1 (0.4) |
23 (9.8) |
1 (0.4) |
|
|
Transtornos Psiquiátricos |
|||||
|
Insomnio |
35 (14.7) |
2 (0.8) |
47 (20.0) |
0 (0.0) |
|
|
Transtornos Respiratorios, Torácicos y Mediastínicos |
|||||
|
Tose |
37 (15.5) |
2 (0.8) |
31 (13.2) |
0 (0.0) |
|
|
Disneaf |
28 (11.8) |
1 (0.4) |
26 (11.1) |
2 (0.9) |
|
|
Transtornos Vasculares |
|||||
|
Hipertensióng |
51 (21.4) |
13 (5.5) |
48 (20.4) |
12 (5.1) |
|
Kd = Kyprolis y dexametasona
a La anemia incluye anemia, disminución del hematocrito y disminución de la hemoglobina.
b La trombocitopenia incluye disminución del recuento de plaquetas y trombocitopenia.
c La neutropenia incluye el recuento de neutrófilos disminuido y neutropenia.
d La infección del tracto respiratorio incluye infección del tracto respiratorio, infección del tracto respiratorio inferior, infección del tracto respiratorio superior e infección del tracto respiratorio superior virald.
e La tos incluye tos y tos productiva.
f La disnea incluye disnea y disnea de esfuerzo.
g La hipertensión incluye hipertensión y crisis hipertensiva.
Reacciones adversas que ocurren a una frecuencia de <10%
- Trastornos sanguíneos y del sistema linfático: neutropenia febril, leucopenia, linfopenia, neutropenia, microangiopatía trombótica.
- Trastornos cardíacos: fibrilación auricular, paro cardíaco, insuficiencia cardíaca, insuficiencia cardíaca congestiva, infarto de miocardio, isquemia miocárdica, palpitaciones, derrame pericárdico, taquicardia.
- Trastornos del oído y laberínticos: tinnitus.
- Trastornos oculares: cataratas, visión borrosa.
- Trastornos gastrointestinales: dolor abdominal, dolor abdominal superior, estreñimiento, dispepsia, dolor de muelas, vómitos.
- Trastornos generales y afecciones en el lugar de administración: dolor en el pecho, escalofríos, enfermedades similares a la influenza, reacciones en el lugar de la infusión (incluida inflamación, dolor y eritema), malestar general, dolor.
- Trastornos hepatobiliares: colestasis, insuficiencia hepática, hiperbilirrubinemia.
- Infecciones: colitis por clostridium difficile, gastroenteritis, influenza, infección pulmonar, nasofaringitis, rinitis, sepsis, shock séptico, infección del tracto urinario, infección viral.
- Trastornos del metabolismo y de la nutrición: disminución del apetito, deshidratación, hipercalcemia, hiperglucemia, hipercalemia, hiperuricemia, hipoalbuminemia, hipocalcemia, hipomagnesemia, hiponatremia, hipofosfatemia, síndrome de lisis tumoral.
- Trastornos musculoesqueléticos y del tejido conjuntivo: espasmos musculares, debilidad muscular, dolor torácico musculoesquelético, dolor musculoesquelético, mialgia.
- Trastornos del sistema nervioso: accidente cerebrovascular, mareos, parestesia, neuropatía periférica.
- Trastornos psiquiátricos: ansiedad, delirio.
- Trastornos renales y urinarios: lesión renal aguda, insuficiencia renal, daño renal
- Trastornos respiratorios, torácicos y mediastínicos: síndrome de dificultad respiratoria aguda, disfonía, epistaxis, enfermedad pulmonar intersticial, dolor orofaríngeo, neumonitis, hemorragia pulmonar, embolia pulmonar, hipertensión pulmonar, edema pulmonar, sibilancias.
- Trastornos de la piel y del tejido subcutáneo: eritema, hiperhidrosis, prurito, erupción cutánea.
- Trastornos vasculares: trombosis venosa profunda, sofocos, hipotensión.
Kyprolis en Combinación con Daratumumab Intravenoso y Dexametasona
La seguridad de Kyprolis en combinación con daratumumab intravenoso y dexametasona se evaluó en dos estudios (CANDOR y EQUULEUS).
CANDOR
La seguridad de Kyprolis 20/56 mg/m2 dos veces a la semana en combinación con daratumumab intravenoso y dexametasona (DKd) se evaluó en CANDOR (Ver Estudios Clínicos). Pacientes recibieron Kyprolis durante una mediana de 58 semanas en el brazo de DKd y de 40 semanas en el brazo de Kd.
Se reportaron reacciones adversas graves en el 56% de los pacientes en el brazo de DKd y en el 46% de los pacientes en el brazo de Kd. Las reacciones adversas graves más frecuentes informadas en el brazo de DKd en comparación con el brazo de Kd fueron neumonía (14% versus 9 %), pirexia (4,2% versus 2,0%), influenza (3.9% versus 1.3%), septicemia (3.9% versus 1.3%), anemia (2.3% versus 0.7%), bronquitis (1.9% versus 0%) y diarrea (1.6% versus 0%). Se produjeron reacciones adversas fatales dentro de los 30 días posteriores a la última dosis de cualquier tratamiento del estudio en un 10% de los 308 pacientes en el brazo de DKd en comparación con un 5% de los 153 pacientes en el brazo de Kd. La reacción adversa fatal más frecuente (DKd versus Kd) fue infección, 4.5% versus 2.6%.
La interrupción permanente del fármaco debido a una reacción adversa en pacientes que recibieron Kyprolis se produjo en un 21 % de los pacientes del brazo de DKd versus un 22% en el brazo de Kd. Las reacciones adversas más frecuentes que llevaron a la interrupción del tratamiento con Kyprolis fueron insuficiencia cardíaca (1.9%) y fatiga (1.9%) en el brazo de DKd e insuficiencia cardíaca (2.0%), hipertensión (2,0%) y lesión renal aguda (2.0%) en el brazo de Kd. Se interrumpió el tratamiento con Kyprolis debido a reacciones adversas en el 71% de los pacientes en el brazo de DKd versus un 63% en el brazo de Kd. Se redujo la dosis de Kyprolis debido a reacciones adversas en el 25% de los pacientes del brazo de DKd versus un 20% en el brazo de Kd.
Se produjeron reacciones relacionadas con la infusión después de a primera dosis de Kyprolis en un 13% en el brazo de DKd versus un 1% en el brazo de Kd.
La Tabla 22 resume las reacciones adversas en CANDOR.
|
Reacciones Adversas |
DKd dos veces a la semana (N = 308) |
Kd dos veces a la semana (N = 153) |
||
|
Todos los grados (%) |
Grados 3 a4 |
Todos los grados (%) |
Grados 3 a 4 |
|
|
Trastornos Generales y Alteraciones en el Lugar de Administración |
||||
|
Reacción relacionada con la infusióna |
41 |
12 |
28 |
5 |
|
Fatigab |
32 |
11 |
28 |
8 |
|
Pirexia |
20 |
1.9 |
15 |
0.7 |
|
Infecciones |
||||
|
Infección del tracto respiratorioc |
40g |
7 |
29 |
3.3 |
|
Neumonía |
18g |
13 |
12 |
9 |
|
Bronquitis |
17 |
2.6 |
12 |
1.3 |
|
Trastornos de la Sangre y del Sistema Linfático |
||||
|
Trombocitopeniad |
37 |
25 |
30 |
16 |
|
Anemiae |
33 |
17 |
31 |
14 |
|
Trastornos Gastrointestinales |
||||
|
Diarrea |
32 |
3.9 |
14 |
0.7 |
|
Náuseas |
18 |
0 |
13 |
0.7 |
|
Trastornos Vasculares |
||||
|
Hipertensión |
31 |
18 |
28 |
13 |
|
Trastornos Respiratorios, Torácicos y Mediastínicos |
||||
|
Tosf |
21 |
0 |
21 |
0 |
|
Disnea |
20 |
3.9 |
22 |
2.6 |
|
Trastornos Psiquiátricos |
||||
|
Insomnio |
18 |
3.9 |
11 |
2.0 |
|
Trastornos Musculoesqueléticos y del Tejido Conjuntivo |
||||
|
Dolor de espalda |
16 |
1.9 |
10 |
1.3 |
DKd = Kyprolis, daratumumab y dexametasona; Kd = Kyprolis y dexametasona
a La incidencia de reacciones relacionadas con la infusión se basa en un conjunto de síntomas (como hipertensión, pirexia, erupción, mialgia, hipotensión, aumento de la presión arterial, urticaria, lesión renal aguda, broncoespasmo, edema de cara, hipersensibilidad, síncope, sibilancia, prurito en el ojo, edema palpebral, insuficiencia renal, hinchazón facial) relacionados con la infusión que se produjeron dentro de 1 día después de la administración de DKd o Kd.
b La fatiga incluye fatiga y astenia.
c La infección del tracto respiratorio incluye infección del tracto respiratorio, infección del tracto respiratorio inferior, infección del tracto respiratorio superior e infección del tracto respiratorio superior viral.
d La trombocitopenia incluye disminución del recuento de plaquetas y trombocitopenia.
e La anemia incluye anemia, disminución del hematocrito y disminución de la hemoglobina.
f La tos incluye tos y tos productiva.
g Incluye reacciones adversas mortales.
Reacciones adversas que ocurren a una frecuencia de < 15%
- Trastornos de la sangre y del sistema linfático: neutropenia febril, púrpura trombocitopénica trombótica.
- Trastornos cardíacos: fibrilación auricular, paro cardíaco, falla cardíaca, cardiomiopatía, infarto al miocardio, isquemia de miocardio, taquicardia.
- Trastornos oculares: cataratas.
- Trastornos gastrointestinales: dolor abdominal, hemorragia gastrointestinal.
- Trastornos generales y alteraciones en el lugar de administración: dolor torácico, malestar.
- Infecciones: gastroenteritis, influenza, infección pulmonar, nasofaringitis, septicemia, shock séptico, infección del tracto urinario, infección viral.
- Exploraciones complementarias: alanina aminotransferasa elevada, creatinina en sangre elevada, proteína C reactiva elevada, fracción de eyección disminuida.
- Trastornos del metabolismo y de la nutrición: deshidratación, hiperglucemia, hipercalemia, hipocalemia, hiponatremia, síndrome de lisis tumoral.
- Trastornos musculoesqueléticos y del tejido conjuntivo: dolor en una extremidad.
- Trastornos del sistema nervioso: accidente cerebrovascular, hemorragia intracraneal, síndrome de encefalopatía posterior reversible, neuropatía periférica.
- Trastornos psiquiátricos: ansiedad.
- Trastornos renales y urinarios: lesión renal aguda, insuficiencia renal, daño renal.
- Trastornos respiratorios, torácicos y mediastínicos: insuficiencia respiratoria aguda, epistaxis, enfermedad pulmonar intersticial, neumonitis, embolismo pulmonar, hipertensión pulmonar, edema pulmonar.
- Trastornos de la piel y del tejido subcutáneo: erupción.
- Trastornos vasculares: trombosis venosa profunda, crisis hipertensiva.
EQUULEUS
La seguridad de Kyprolis 20/70 mg/m2 una vez a la semana en combinación con daratumumab y dexametasona (DKd) se evaluó en EQUULEUS (ver Estudios Clínicos). Los pacientes recibieron Kyprolis por una mediana de duración de 66 semanas.
Se informaron reacciones adversas graves en un 48% de los pacientes. Las reacciones adversas graves más frecuentes fueron neumonía (4.7%), infección del tracto respiratorio superior (4.7%), carcinoma basocelular (4.7%), influenza (3.5%), deterioro general del estado físico (3.5%) e hipercalcemia (3.5%). Se produjeron reacciones adversas mortales dentro de los 30 días de la última dosis de cualquier tratamiento del estudio en un 3.5% de los pacientes, que murieron de deterioro general del estado físico, falla orgánica múltiple después de aspergilosis pulmonar y progresión de la enfermedad.
Se produjo discontinuación del tratamiento con Kyprolis en un 19% de los pacientes. La reacción adversa más frecuente que llevó a la interrupción del tratamiento fue la astenia (2%). Se produjo la interrupción del tratamiento de Kyprolis debido a reacciones
adversas en un 77% de los pacientes. Se produjo la reducción de la dosis de Kyprolis debido reacciones adversas en un 31% de los pacientes en DKd.
Las reacciones relacionadas con la infusión que se produjeron después de la primera dosis de Kyprolis fueron de un 11%. Se informó de reacciones adversas de hipertensión pulmonar en un 4.7% de los pacientes en EQUULEUS.
La Tabla 23 resume las reacciones adversas en EQUULEUS.
Tabla 23: Reacciones Adversas(≥ 15%) en Pacientes que Recibieron Dkd (Régimen de 20/70 mg/m2) en EQUULEUS
|
Reacciones Adversas |
DKd una vez a la semana (N = 85) |
|
|
Todos los grados (%) |
Grados 3 a 4 (%) |
|
|
Trastornos de la Sangre y del Sistema Linfático |
||
|
Trombocitopeniaa |
68 |
32 |
|
Anemiab |
52 |
21 |
|
Neutropeniac |
31 |
21 |
|
Linfopeniad |
29 |
25 |
|
Trastornos Generales y Alteraciones en el Lugar de Administración |
||
|
Fatioae |
54 |
18 |
|
Reacción relacionada con la infusiónf |
53 |
12 |
|
Pirexia |
37 |
1.2 |
|
Infecciones |
||
|
Infección del tracto respiratoriog |
53 |
3.5 |
|
Bronquitis |
19 |
0 |
|
Nasofaringitis |
18 |
0 |
|
Influenza |
17 |
3.5 |
|
Trastornos Gastrointestinales |
||
|
Náuseas |
42 |
1.2 |
|
Vómito |
40 |
1.2 |
|
Diarrea |
38 |
2.4 |
|
Constipación |
17 |
0 |
|
Trastornos Respiratorios, Torácicos y Mediastínicos |
||
|
Disnea |
35 |
3.5 |
|
Tosh |
33 |
0 |
|
Trastornos Vasculares |
||
|
Hipertensión |
33 |
20 |
|
Trastornos Psiquiátricos |
||
|
Insomnio |
33 |
4.7 |
|
Trastornos del sistema nervioso |
||
|
Dolor de cabeza |
27 |
1.2 |
|
Trastornos Musculoesqueléticos y del Tejido Conjuntivo |
||
|
Dolor de espalda |
25 |
0 |
|
Dolor en una extremidad |
15 |
0 |
DKd = Kyprolis, daratumumab y dexametasona; Kd = Kyprolis y dexametasona
a La trombocitopenia incluye disminución de recuento de plaquetas y trombocitopenia.
b La anemia incluye anemia, disminución del hematocrito y disminución de la hemoglobina.
c La neutropenia incluye el recuento de neutrófilos disminuido y neutropenia.
d La linfopenia incluye recuento de linfocitos disminuido y linfopenia.
e La fatiga incluye fatiga y astenia.
f La incidencia de reacciones relacionadas con la infusión se basa en un conjunto de síntomas (como hipertensión, pirexia, erupción, mialgia, hipotensión, aumento de la presión arterial, urticaria, lesión renal aguda, broncoespasmo, edema de cara, hipersensibilidad, síncope, sibilancia, prurito en el ojo, edema palpebral, insuficiencia renal, edema facial) relacionados con la infusión que se produjeron dentro de 1 día después de la administración de DKd.
g La infección del tracto respiratorio incluye infección del tracto respiratorio, infección del tracto respiratorio inferior, infección del tracto respiratorio superior e infección del tracto respiratorio superior viral.
h La tos incluye tos y tos productiva.
Reacciones adversas que ocurren a una frecuencia de < 15%
- Trastornos de la sangre y del sistema linfático: neutropenia febril, microangiopatía trombótica.
- Trastornos cardíacos: insuficiencia cardíaca, isquemia de miocardio.
- Trastornos gastrointestinales: dolor abdominal.
- Trastornos generales y alteraciones en el lugar de administración: síndrome de disfunción multiorgánica.
- Infecciones: neumonía, septicemia, shock séptico.
- Trastornos del metabolismo y de la nutrición: deshidratación, hipercalcemia.
- Trastornos renales y urinarios: lesión renal aguda, insuficiencia renal, daño renal.
- Trastornos respiratorios, torácicos y mediastínicos: embolismo pulmonar, hipertensión pulmonar.
- Trastornos vasculares: hipotensión.
Kyprolis en Pacientes que Recibieron Monoterapia
La seguridad de Kyprolis 20/27 mg/m2 como una infusión de 10 minutos fue evaluada en estudios clínicos en 598 pacientes con mieloma en recaída y/o refractario (ver Estudios Clínicos). Se requirió pre-medicar dexametasona 4 mg antes de cada dosis en el Ciclo 1 y fue opcional para subsecuentes ciclos. La mediana de edad fue 64 años (rango 32 a 87), y aproximadamente 57% fueron hombres. Los pacientes recibieron una mediana de 5 (rango 1 a 20) regímenes previos. La mediana del número de ciclos iniciados fue 4 (rango 1 a 35).
Ocurrieron muertes debidas a reacciones adversas dentro de los 30 días desde la última dosis de Kyprolis en 30/598 (5%) pacientes que recibieron monoterapia con Kyprolis. Estas reacciones adversas estuvieron relacionadas a trastornos cardiacos en 10 (2%) pacientes, infecciones en 8 (1%) pacientes, trastornos renales en 4 (< 1%) pacientes, y otras reacciones adversas en 8 (1%) pacientes.
Se reportaron reacciones adversas graves, sin importar la causalidad, en el 50% de los pacientes en los estudios agrupados de monoterapia con Kyprolis (N = 598). Las reacciones adversas graves más frecuentes fueron: neumonía (8%), insuficiencia renal aguda (5%), progresión de la enfermedad (4%), pirexia (3%), hipercalcemia (3%), insuficiencia cardíaca congestiva (3%), mieloma múltiple (3%), anemia (2%) y disnea (2%).
En FOCUS, un estudio aleatorizado que comparó Kyprolis como agente único versus corticoides con ciclofosfamida oral opcional para pacientes con mieloma múltiple en recaída o refractario, la mortalidad fue mayor en los pacientes tratados con Kyprolis en comparación al brazo de control en el subgrupo de 48 pacientes de ≥ 75 años de edad. La causa más común de discontinuación debida a una reacción adversa fue insuficiencia renal aguda (2%).
La seguridad de la monoterapia con Kyprolis dosificado a 20/56 mg/m2 mediante una infusión de 30 minutos fue evaluada en un estudio multicéntrico y abierto en pacientes con mieloma múltiple en recaída y/o refractario (ver Estudios Clínicos). Los pacientes recibieron una mediana de 4 (rango 1 a 10) regímenes previos.
Las reacciones adversas que ocurren con la monoterapia con Kyprolis se presentan en la Tabla 24.
Tabla 24: Reacciones Adversas Más Comunes (≥ 20%) con Monoterapia de Kyprolis
|
Reacción Adversa |
20/56 mg/m2 |
20/27 mg/m2 |
||
|---|---|---|---|---|
|
Todos los grados |
Grados 3 a 5 |
Todos los grados |
Grados |
|
|
Fatiga |
14 (58) |
2 (8) |
238 (40) |
25 (4) |
|
Disneaa |
14 (58) |
2 (8) |
202 (34) |
21 (4) |
|
Pirexia |
14 (58) |
0 |
177 (30) |
11 (2) |
|
Trombocitopenia |
13 (54) |
13 (54) |
220 (37) |
152 (25) |
|
Náusea |
13 (54) |
0 |
211 (35) |
7 (1) |
|
Anemia |
10 (42) |
7 (29) |
291 (49) |
141 (24) |
|
Hipertensiónb |
10 (42) |
3 (13) |
90 (15) |
22 (4) |
|
Escalofrío |
9 (38) |
0 |
73 (12) |
1 (< 1) |
|
Cefalea |
8 (33) |
0 |
141 (24) |
7 (1) |
|
Tosc |
8 (33) |
0 |
134 (22) |
2 (< 1) |
|
Vómito |
8 (33) |
0 |
104 (17) |
4 (1) |
|
Linfopenia |
8 (33) |
8 (33) |
85 (14) |
73 (12) |
|
Insomnio |
7 (29) |
0 |
75 (13) |
0 |
|
Mareo |
7 (29) |
0 |
64 (11) |
5 (1) |
|
Diarrea |
6 (25) |
1 (4) |
160 (27) |
8 (1) |
|
Incremento de creatinina en sangre |
6 (25) |
1 (4) |
103 (17) |
15 (3) |
|
Edema periférico |
5 (21) |
0 |
118 (20) |
1 (< 1) |
|
Dolor de espalda |
5 (21) |
1 (4) |
115 (19) |
19 (3) |
|
Infección del tracto respiratorio superior |
5 (21) |
1 (4) |
112 (19) |
15 (3) |
|
Disminución de apetito |
5 (21) |
0 |
89 (15) |
2 (< 1) |
|
Espasmos musculares |
5 (21) |
0 |
62 (10) |
2 (< 1) |
|
Dolor de pecho |
5 (21) |
0 |
20 (3) |
1 (< 1) |
a Disnea incluye disnea y disnea por esfuerzo.
b Hipertensión incluye hipertensión, crisis hipertensiva, y emergencia hipertensiva.
c Tos incluye tos y tos productiva.
Reacciones Adversas que Ocurren a una Frecuencia de < 20%
- Trastornos de la sangre y del sistema linfático: neutropenia febril, leucopenia, neutropenia.
- Trastornos cardiacos: paro cardiaco, falla cardiaca, insuficiencia cardiaca congestiva, infarto al miocardio, isquemia de miocardio.
- Trastornos del oído y laberínticos: tinnitus.
- Trastornos oculares: catarata, visión borrosa.
- Trastornos gastrointestinales: dolor abdominal, dolor abdominal superior, estreñimiento, dispepsia, hemorragia gastrointestinal, dolor de muelas.
- Trastornos generales y alteraciones en el lugar de administración: astenia, reacción en el sitio de infusión, falla orgánica múltiple, dolor.
- Trastornos hepatobiliares: falla hepática.
- Infecciones: bronquitis, bronconeumonía, influenza, infección pulmonar, neumonía, nasofaringitis, infección del tracto respiratorio, rinitis, septicemia, infección del tracto urinario.
- Trastornos del metabolismo y de la nutrición: hipercalcemia, hiperglucemia, hipercalemia, hiperuricemia, hipoalbuminemia, hipocalcemia, hipocalemia, hipomagnesemia, hiponatremia, hipofosfatemia, síndrome de lisis tumoral.
- Trastornos musculoesqueléticos y de tejido conjuntivo: artralgia, dolor musculoesquelético, dolor musculoesquelético de pecho, mialgia, dolor en extremidades.
- Trastornos del sistema nervioso: hipoestesia, hemorragia intracraneal, parestesia, neuropatía periférica motora, neuropatía periférica, neuropatía periférica sensorial.
- Trastornos psiquiátricos: ansiedad.
- Trastornos renales y urinarios: insuficiencia renal aguda, insuficiencia renal, daño renal.
- Trastornos respiratorios, torácicos y mediastínicos: disfonía, epistaxis, dolor orofaríngeo, edema pulmonar, hemorragia pulmonar.
- Trastornos de la piel y del tejido subcutáneo: eritema, hiperhidrosis, prurito, erupción.
- Trastornos vasculares: eventos embólicos y trombóticos, venosos (incluyendo trombosis venosa profunda y embolismo pulmonar), hemorragia hipotensión.
Reacciones adversas Grado 3 o mayor ocurriendo con una incidencia de > 1% incluyen neutropenia febril, paro cardiaco, insuficiencia cardiaca congestiva, dolor, sepsis, infección del tracto urinario, hiperglucemia, hipercalemia, hiperuricemia, hipoalbuminemia, hipocalcemia, hiponatremia, hipofosfatemia, insuficiencia renal, insuficiencia renal aguda, daño renal, edema pulmonar, e hipotensión.
La Tabla 25 describe las anormalidades de laboratorio Grado 3 a 4 reportadas en una tasa de > 10% para pacientes que recibieron monoterapia de Kyprolis.
Tabla 25: Anormalidades de Laboratorio Grado 3 a 4 (> 10%) con Monoterapia de Kyprolis
|
Anormalidad de Laboratorio |
Kyprolis |
Kyprolis |
|---|---|---|
|
Disminución de linfocitos |
15 (63) |
151 (25) |
|
Disminución de plaquetas |
11 (46) |
184 (31) |
|
Disminución de hemoglobina |
7 (29) |
132 (22) |
|
Disminución de la cuenta total de glóbulos blancos |
3 (13) |
71 (12) |
|
Disminución de sodio |
2 (8) |
69 (12) |
|
Disminución de la cuenta absoluta de neutrófilos |
2 (8) |
67 (11) |
Experiencia Post-comercialización
Las siguientes reacciones adversas adicionales fueron reportadas en la experiencia post-comercialización con Kyprolis. Dado que estas reacciones son reportadas de forma voluntaria en una población de tamaño incierto, no siempre es posible estimar de forma confiable su frecuencia o establecer una relación causal con la exposición al fármaco: síndrome hemolítico urémico (HUS, por sus siglas en inglés), reactivación de virus de hepatitis B, perforación gastrointestinal, pericarditis e infección por citomegalovirus, incluyendo coriorretinitis, neumonitis, enterocolitis, viremia, obstrucción intestinal y pancreatitis aguda.
Uso en poblaciones específicas
Uso Pediátrico
La seguridad y efectividad de Kyprolis en pacientes pediátricos no ha sido establecida.
Uso Geriátrico
De los 2387 pacientes en estudios clínicos de Kyprolis, el 51% tenía 65 años o más, mientras que el 14% tenía 75 años o más. La incidencia de eventos adversos graves fue del 49% en pacientes de< 65 años de edad, del 58% en pacientes de 65 a 74 años de edad, y del 63% en pacientes de ≥ 75 años de edad. De los 308 pacientes en CANDOR que recibieron DKd, un 47% tenía 65 años o una edad superior, mientras que un 9% tenía 75 años o una edad superior. Se produjeron reacciones adversas fatales en el brazo de DKd de CANDOR en un 6% de los pacientes de< 65 años, un 14% de los pacientes entre 65 y 74 años y un 14% de los pacientes de ≥ 75 años (ver Reacciones secundarias y adversas). No se observaron diferencias generales en la efectividad entre los pacientes mayores y los más jóvenes.
Daño Hepático
Reducir la dosis de Kyprolis en un 25% en pacientes con daño hepático leve (bilirrubina total 1 a 1.5 ×ULN o cualquier AST o bilirrubina total ≤ ULN y AST > ULN) o moderada (bilirrubina total > 1.5 a 3 ×ULN y cualquier AST). No se puede recomendar una dosis para pacientes con función hepática severa. (ver Dosis y vía de administración y Farmacocinética).
La incidencia de eventos adversos graves fue mayor en pacientes con insuficiencia hepática leve, moderada y grave combinados (22/35 o 63%) que en pacientes con función hepática normal (3/11 o 27%) (ver Precauciones generales y Farmacocinética).
Para inyección: 60 mg polvo liofilizado en un frasco ámpula de una sola dosis para reconstitución.
Cálculo de Dosis
Para pacientes con un área de superficie corporal (BSA, por sus siglas en inglés) de 2.2 m2 o menos, calcule la dosis de Kyprolis con el BSA real. No se necesita hacer ajustes para cambios de peso menor o iguales al 20%.
En pacientes con un BSA superior a 2.2 m2, calcule la dosis de Kyprolis con un BSA de 22 m2.
Dosis Recomendada
Kyprolis en Combinación con Lenalidomida y Dexametasona
Administrar Kyprolis vía intravenosa mediante una infusión de 1 mInu os en os ías 1, 2, 8, 9, 15 y 16 de cada ciclo de 28 días en combinación con lenalidomida y dexametasona hasta el Ciclo 12, como se muestra en la Tabla 26 (ver Estudios Clínicos). La dosis inicial recomendada de Kyprolis es de 20 mg/m2 en el Ciclo 1, Días 1 y 2. De ser tolerado, la dosis deberá escalarse a 27 mg/m2 en el Ciclo 1, Día 8. Desde el Ciclo 13, administrar Kyprolis en los Días 1, 2, 15, 16 hasta el Ciclo 18. Suspender Kyprolis después del Ciclo 18. Continuar con la lenalidomida y la dexametasona hasta que se produzca la progresión de la enfermedad o una toxicidad inaceptable. Ver la Información para Prescribir de la lenalidomida y la dexametasona para obtener información adicional sobre la dosis.
Tabla 26: Kyprolis 20/27 mg/m2 Dos veces por Semana (Infusión de 10 Minutos) en Combinación con Lenalidomida y Dexamentasona
|
|
Ciclo 1 |
||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana4 |
||||||||
|
Día 1 |
Día 2 |
Días 3 a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 1 6 |
Días 1 7 a 21 |
Día 2 2 |
Días 23 a 28 |
|
|
Kyprolis (mg/m2) |
20 |
20 |
- |
27 |
27 |
- |
27 |
27 |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
|
Lenali-domida |
25 mg diariamente en los Días 1 a 21 |
- |
- |
||||||||
|
|
Ciclos 2 a 12 |
||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana4 |
||||||||
|
Día 1 |
Día 2 |
Días 3 a7 |
Día 8 |
Día 9 |
Días 10 a14 |
Día 15 |
Día 1 6 |
Días 1 7 a 21 |
Día 2 2 |
Días 23 a 28 |
|
|
Kyprolis (mg/m2) |
27 |
27 |
- |
27 |
27 |
- |
27 |
27 |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
|
Lenali-domida |
25 mg diariamente en los Días 1 a 21 |
- |
- |
||||||||
|
|
Ciclos 13 y posterioresa |
||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana4 |
||||||||
|
Día 1 |
Día 2 |
Días 3 a7 |
Día 8 |
Día 9 |
Días 10 a14 |
Día 15 |
Día 1 6 |
Días 1 7 a 21 |
Día 2 2 |
Días 23 a 28 |
|
|
Kyprolis (mg/m2) |
27 |
27 |
- |
27 |
27 |
- |
27 |
27 |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
|
Lenali-domida |
25 mg diariamente en los Días 1 a 21 |
- |
- |
||||||||
a Kyprolis es administrado hasta el Ciclo 18, la lenalidomida y la dexametasona continúan a partir de esa semana.
Kyprolis en Combinación con Dexametasona
Régimen de 20/56 mg.r/m2 dos veces par semana mediante infusión de 30 minutos
Administrar Kyprolis vía intravenosa como una infusión de 30 minutos en los Días 1, 2, 8, 9, 15 y 16 de cada ciclo de 28 días en combinación con dexametasona hasta la progresión de la enfermedad o hasta una toxicidad inaceptable, como se muestra en la Tabla 27 (ver Estudios Clínicos). La dosis inicial recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1, Días 1 y 2. Si se tolera, escalar la dosis a 56 mg/m2 en el Ciclo 1, Día 8. Administrar dexametasona de 30 minutos a 4 horas antes de Kyprolis. Referir a la Información para Prescribir de dexametasona a fin de obtener información adicional sobre la dosis.
Tabla 27: Kyprolis 20/56 mg/m2 Dos Veces a la Semana (Infusión de 30 minutos) en Combinación con Dexametasona
|
|
Ciclo 1 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día |
Día |
Días |
Día |
Día |
Días |
Día |
Día |
Días |
Día |
Día |
Días |
|
|
Kyprolis (mg/m2) |
20 |
20 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
- |
- |
|
Dexametasona (mg) |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
|
|
Ciclos 2 y posteriores |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día |
Día |
Días |
Día |
Día |
Días 10 a 14 |
Día |
Día |
Días |
Día |
Día |
Días |
|
|
Kyprolis (mg/m2) |
56 |
56 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
- |
- |
|
Dexametasona (mg) |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
Una vez por semana un régimen de 20170 mg/m2 mediante infusión de 30 minutos
Administrar Kyprolis vía intravenosa como una infusión de 30 minutos en los Días 1, 8 y 15 de cada ciclo de 28 días en combinación con dexametasona hasta la progresión de la enfermedad o hasta una toxicidad inaceptable, como se muestra en la Tabla 28 (ver Estudios Clínicos). La dosis inicial recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1, Día 1. Si se tolera, escalar la dosis a 70 mg/m2 en el Ciclo 1, Día 8. Administrar dexametasona de 30 minutos a 4 horas antes de Kyprolis. Ver la Información para Prescribir de dexametasona a fin de obtener información adicional sobre la dosis.
Tabla 28: Kyprolis 20/70 mg/m2 Una Vez a la Semana (Infusión de 30 Minutos) en Combinación con Dexametasona
|
|
Ciclo 1 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24 a 28 |
|
|
Kyprolis (mg/m2) |
20 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
|
Ciclos 2 a 9 |
||||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 22 |
Días 24 a 28 |
|
|
Kyprolis (mg/m2) |
70 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
|
Ciclos 10 y posteriores |
||||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 22 |
Días 24 a 28 |
|
|
Kyprolis (mg/m2) |
70 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg) |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
- |
- |
- |
Kyprolis en combinación con daratumumab intravenoso y dexametasona
Régimen de 20/56 mglm2 dos veces por semana mediante infusión de 30 minutos
Administrar Kyprolis por vía intravenosa como una infusión de 30 minutos los Días 1, 2, 8, 9, 15 y 16 de cada ciclo de 28 días en combinación con daratumumab intravenoso y dexametasona hasta la progresión de la enfermedad o una toxicidad inaceptable, como se muestra en la Tabla 29 (ver Estudios Clínicos). La dosis inicial recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1, Días 1 y 2. De ser tolerado, la dosis deberá escalarse a 56 mg/m2 en el Ciclo 1, Día 8, y de ahí en adelante. Administrar dexametasona de 30 minutos a 4 horas antes de Kyprolis y de 1 a 3 horas antes del daratumumab intravenoso. Ver la Información para Prescribir de daratumumab intravenoso y dexametasona si desea obtener información adicional sobre la dosis.
Tabla 29: Kyprolis 20/56 mg/m2 Dos Veces por Semana (Infusión de 30 Minutos) en Combinación con Daratumumab Intravenoso y Dexametasona
|
|
Ciclo 1 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
|
Kyprolis (mg/m2) |
20 |
20 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
40 |
- |
- |
|
Daratumumab (mg/kg) |
8 |
8 |
- |
16 |
- |
- |
16 |
- |
- |
16 |
- |
- |
|
|
Ciclos 3 a 6 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
|
Kyprolis (mg/m2) |
56 |
56 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
40 |
- |
- |
|
Daratumumab (mg/kg) |
16 |
- |
- |
- |
- |
- |
16 |
- |
- |
- |
- |
- |
|
|
Ciclos 7 y posteriores |
|||||||||||
|
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
||||||||
|
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
Kyprolis (mg/m2) |
56 |
56 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
40 |
- |
- |
|
Daratumumab (mg/kg) |
16 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
* En pacientes mayores de 75 años, administre 20 mg de dexametasona por vía oral o intravenosa una vez a la semana después de la primera semana.
Régimen de 20/70 mg/m2 una vez por semana mediante infusión de 30 minutos
Administrar Kyprolis por vía intravenosa como una infusión de 30 minutos los Días 1, 8 y 15 de cada ciclo de 28 días en combinación con daratumumab intravenoso y dexametasona hasta la progresión de la enfermedad o una toxicidad inaceptable, como se muestra en la Tabla 30 (ver Estudios Clínicos). La dosis inicial recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1, Día 1. De ser tolerado, la dosis deberá escalarse a 70 mg/m2 en el Ciclo 1, Día 8, y de ahí en adelante. Administrar dexametasona de 30 minutos a 4 horas antes de Kyprolis y de 1 a 3 horas antes del daratumumab intravenoso. Ver la Información para Prescribir de daratumumab intravenoso y dexametasona si desea obtener información adicional sobre la dosis.
Tabla 30: Kyprolis 20/70 mg/m2 Una Vez a la Semana (Infusión de 30 Minutos) en Combinación con Daratumumab intravenoso y Dexametasona
|
|
Ciclo 1 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
|
Kyprolis (mg/m2) |
70 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
20 |
20 |
- |
|
Daratumumab (mg/kg) |
16 |
- |
- |
16 |
- |
- |
16 |
- |
- |
16 |
- |
- |
|
|
Ciclos 3 a 6 |
|||||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||||
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
|
Kyprolis (mg/m2) |
70 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
40 |
- |
- |
20 |
20 |
- |
40 |
- |
- |
|
Daratumumab (mg/kg) |
16 |
- |
- |
- |
- |
- |
16 |
- |
- |
- |
- |
- |
|
|
Ciclos 7 y posteriores |
|||||||||||
|
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
||||||||
|
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Día 22 |
Día 23 |
Días 24a 28 |
|
Kyprolis (mg/m2) |
70 |
- |
- |
70 |
- |
- |
70 |
- |
- |
- |
- |
- |
|
Dexametasona (mg)* |
20 |
20 |
- |
40 |
- |
- |
40 |
- |
- |
40 |
- |
- |
|
Daratumumab (mg/kg) |
16 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
* En pacientes mayores de 75 años, administre 20 mg de dexametasona por vía oral o intravenosa una vez a la semana después de la primera semana.
Monoterapia con Kyprolis
Régimen de 20/27 mglm2 dos veces por semana mediante infusión de 10 minutos
Administrar Kyprolis vía intravenosa mediante una infusión de 10 minutos (ver Estudios Clínicos). En los Ciclos 1 hasta el 12, administrar Kyprolis en los Días 1, 2, 8, 9, 15 y 16 de cada ciclo de 28 días como se muestra en la Tabla 31. A partir del Ciclo 13, administrar Kyprolis en los Días 1, 2, 15 y 16 de cada ciclo de 28 días. Pre-medicar con dexametasona 4 mg oral o intravenoso 30 minutos a 4 horas antes de cada dosis de Kyprolis en el Ciclo 1, posteriormente según se requiera para minimizar las reacciones de la infusión. La dosis inicial recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1 en los Días 1 y 2. Si se tolera, escalar la dosis a 27 mg/m2 en el Día 8 del Ciclo 1 y de ahí en adelante. Continuar con Kyprolis hasta la progresión de la enfermedad o una toxicidad inaceptable.
Tabla 31: Monoterapia con Kyprolis 20/27 mg/m2 Dos veces por Semana (Infusión de 10 Minutos)
|
|
Ciclo 1 |
|||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22 a 28 |
|
|
Kyprolis (mg/m2)a |
20 |
20 |
- |
27 |
27 |
- |
27 |
27 |
- |
- |
|
|
Ciclos 2 a 12 |
|||||||||
|
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
||||||
|
|
Día 1 |
Día 2 |
Días 3a7 |
Día8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22 a 28 |
|
Kyprolis (mg/m2) |
27 |
27 |
- |
27 |
27 |
- |
27 |
27 |
- |
- |
|
|
Ciclos 13 y posteriores |
|||||||||
|
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
||||||
|
|
Día 1 |
Día 2 |
Días 3a7 |
Día8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22 a 28 |
|
Kyprolis (mg/m2) |
27 |
27 |
- |
- |
- |
- |
27 |
27 |
- |
- |
a Se requiere pre-medicación con dexametasona para cada dosis de Kyprolis en el Ciclo 1.
Régimen de 20/56 mg/m2 dos veces por semana mediante infusión de 30 minutos
Administrar Kyprolis vía intravenosa mediante una infusión de 30 minutos (ver Estudios Clínicos). En los Ciclos 1 hasta el 12, administrar Kyprolis en los Días 1, 2, 8, 9, 15 y 16 de cada ciclo de 28 días como lo muestra la Tabla 32. Desde el Ciclo 13, administrar Kyprolis en los Días 1, 2, 15 y 16 de cada ciclo de 28 días. Pre-medicar con dexametasona 8 mg oral o intravenosa 30 minutos a 4 horas antes de cada dosis de Kyprolis en el Ciclo 1, posteriormente según se requiera para minimizar las reacciones de la infusión. La dosis de arranque recomendada de Kyprolis es 20 mg/m2 en el Ciclo 1 en los Días 1 y 2. Si se tolera, escalar la dosis a 56 mg/m2 en el Día 8 del Ciclo 1. Continuar con Kyprolis hasta la progresión de la enfermedad o una toxicidad inaceptable.
Tabla 32: Monoterapia con Kyprolis 20/56 mg/m2 Dos veces por Semana (Infusión de 30 Minutos)
|
|
Ciclo 1 |
|||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana 4 |
|||||||
|
Día 1 |
Día 2 |
Días 3 a 7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22 a 28 |
|
|
Kyprolis (mg/m2)a |
20 |
20 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
|
|
Ciclos 2 a 12 |
|||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana4 |
|||||||
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22a 28 |
|
|
Kyprolis (mg/m2) |
56 |
56 |
- |
56 |
56 |
- |
56 |
56 |
- |
- |
|
|
Ciclos 13 y posteriores |
|||||||||
|
Semana 1 |
Semana 2 |
Semana 3 |
Semana4 |
|||||||
|
Día 1 |
Día 2 |
Días 3a7 |
Día 8 |
Día 9 |
Días 10 a 14 |
Día 15 |
Día 16 |
Días 17 a 21 |
Días 22 a 28 |
|
|
Kyprolis (mg/m2) |
56 |
56 |
- |
- |
- |
- |
56 |
56 |
- |
- |
a Se requiere pre-medicación con dexametasona para cada dosis de Kyprolis en el Ciclo 1.
Precauciones de administración
Hidratación
Se requiere una hidratación adecuada antes de la dosificación en el Ciclo 1, especialmente en pacientes con alto riesgo de síndrome de lisis tumoral o toxicidad renal. La hidratación recomendada incluye tanto líquidos orales (30 mL por kg por lo menos 48 horas antes del Ciclo 1, Día 1) como líquidos por vía intravenosa (250 mL a 500 mL de solución intravenosa apropiada antes de cada una de las dosis del Ciclo 1). Si se requiere, administre adicionalmente de 250 mL a 500 mL de solución por vía intravenosa después de la administración de Kyprolis. Continuar con la hidratación por vía intravenosa y/o oral, según sea necesario en los ciclos posteriores.
Monitorizar a los pacientes por evidencia de sobrecarga de volumen y ajustar la hidratación a las necesidades individuales del paciente, especialmente en pacientes con o en riesgo de insuficiencia cardiaca (consulte Precauciones generales).
Monitorización de electrolitos
Durante el tratamiento con Kyprolis se deberá monitorizar regularmente los niveles de potasio sérico (ver Reacciones secundarias y adversas).
Premedicaciones y medicamentos concomitantes
Pre medicar con la dosis recomendada de dexametasona para monoterapia o con la dosis recomendada de dexametasona si está en terapia en combinación. Administrar dexametasona vía oral o intravenosa por lo menos 30 minutos, pero no más de 4 horas antes de todas las dosis de Kyprolis durante el Ciclo 1 para reducir la incidencia y gravedad de las reacciones a la infusión (ver Precauciones generales). Reinicie la premedicación con dexametasona si se presentan estos síntomas durante los ciclos subsecuentes.
Proporcione tromboprofilaxis para los pacientes tratados con Kyprolis en combinación con otras terapias (ver Precauciones generales).
Se debe considerar la profilaxis antiviral para reducir el riesgo de reactivación del herpes zoster (ver Reacciones secundarias y adversas).
Modificaciones de la Dosis para Reacciones Adversas
En la Tabla 33 se muestran las medidas y modificaciones de dosis recomendadas para Kyprolis. Las reducciones en el nivel de dosis se presentan en la Tabla 34. Ver la Información para Prescribir de lenalidomida, daratumumab intravenoso y dexametasona, respectivamente, para ver las modificaciones recomendadas de dosificación asociadas con cada producto.
Tabla 33: Modificaciones de la Dosis para Reacciones Adversas
|
Toxicidad Hematológica |
Medidas Recomendadas |
|---|---|
|
|
|
|
|
|
|
Toxicidad Renal (ver Precauciones generales) |
Medidas Recomendadas |
|
|
|
Otra Toxicidad No-hematológica (ver Reacciones secundarias y adversas) |
Medida Recomendada |
|
|
CAN = cuenta absoluta de neutrófilos
a Ver Tabla 34 para reducciones del nivel de la dosis.
b Grados 3 y 4.
Tabla 34: Reducciones del Nivel de la Dosis para la toxicidad de Kyprolis
|
Régimen |
Dosis |
Primera Reducción de la Dosis |
Segunda Reducción de la Dosis |
Tercera Reducción de la Dosis |
|
Kyprolis y Dexametasona, (una vez por semana) |
70 mg/m2 |
56 mg/m2 |
45 mg/m2a |
36 mg/m2a |
|
Kyprolis y Dexametasona, o Monoterapia (dos veces por semana) |
56 mg/m2 |
45 mg/m2 |
36 mg/m2 |
27 mg/m2a |
|
Kyprolis, Lenalidomida y Dexametasona, o Monoterapia (dos veces por semana) |
27 mg/m2 |
20 mg/m2 |
15 mg/m2a |
---- |
Nota: Los tiempos de infusión permanecen sin cambio durante la (s) reducción(es) en la dosis.
a Si la toxicidad persiste, descontinuar el tratamiento con Kyprolis.
Modificación de Dosis para Daño Hepático
Para pacientes con daño hepático leve (bilirrubina total 1 a 1.5 x ULN o cualquier AST o bilirrubina total :s; ULN y AST > ULN) o moderado (bilirrubina total > 1.5 a 3 x ULN y cualquier AST), reduzca la dosis de Kyprolis en 25% (ver Uso en poblaciones específicas y farmacocinética).
Dosificación Recomendada para Enfermedad Renal en Etapa Terminal
Para pacientes con enfermedad renal en etapa final quienes están en hemodiálisis, administrar Kyprolis después del procedimiento de hemodiálisis.
Preparación y Administración
Los frascos ámpula de Kyprolis no contienen conservadores antimicrobianos y están previstos para un solo uso. Los viales sin abrir de Kyprolis son estables hasta la fecha indicada en el paquete cuando se almacenan en el empaque original entre 2°C y 8°C (36°F a 46°F). La solución reconstituida contiene carfilzomib a una concentración de 2 mg/mL.
Lea las instrucciones de preparación completas antes de la reconstitución. Los medicamentos parenterales deben inspeccionarse visualmente en busca de partículas y decoloración antes de la administración, siempre que la solución y el envase lo permita.
Reconstitución/Pasos de Preparación:
1. Retirar el frasco ámpula del refrigerador justo antes de usarse.
2. Calcule la dosis (mg/m2) y el número de frascos ámpula de Kyprolis requeridos utilizando el área de la superficie corporal del paciente (BSA) basal.
3. Utilice una aguja de calibre 21 o mayor (aguja con diámetro externo de 0.8 mm o menor) para reconstituir de manera aséptica cada frasco ámpula inyectando lentamente 29 mL (para un frasco ámpula de 60 mg) de Agua Estéril para Inyección, a través del tapón y dirigiendo la solución HACIA LA PARED INTERIOR DEL FRASCO ÁMPULA para minimizar la formación de espuma. (No reconstituir Kyprolis con solución salina normal). No hay datos que respalden el uso de dispositivos de transferencia de sistema cerrado con Kyprolis.
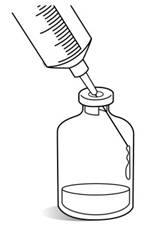
4. Gire y/o invierta suavemente el frasco ámpula despacio por cerca de 1 minuto, o hasta la disolución completa. NO AGITE para evitar generar espuma. Si se ve espuma, permita que la solución se asiente en el frasco ámpula hasta que la espuma desaparezca (aproximadamente 5 minutos) y la solución este clara.
5. Inspeccione visualmente para detección de partículas o cualquier cambio de color previo a la administración. El producto reconstituido debe ser una solución clara e incolora, y no debe administrarse si se observa cualquier cambio de coloración o partículas.
6. Deseche cualquier porción no utilizada que quede en el frasco ámpula. NO combine las porciones no utilizadas de los frascos ámpula. NO administre más de una dosis del frasco ámpula.
7. Administre Kyprolis directamente por infusión intravenosa o de manera opcional, ser administrado en una bolsa intravenosa de 50 mL o 100 mL con Dextrosa al 5% Inyectable. No debe ser administrado como bolo intravenoso.
8. Cuando se administre en una bolsa intravenosa, utilice una aguja de calibre 21 o mayor (aguja con diámetro externo de 0.8 mm o menor) para retirar del frasco ámpula la dosis calculada y diluya en una bolsa intravenosa de 50 mL o 100 mL con Dextrosa al 5% Inyectable, (con base en la dosis total calculada y el tiempo de infusión). No diluya Kyprolis con solución salina normal.
9. Purgue la vía de administración intravenosa con solución salina normal o con Dextrosa al 5%, inmediatamente antes y después de la administración de Kyprolis.
10. No mezcle Kyprolis ni lo administre mediante una infusión con otros medicamentos.
Las estabilidades de Kyprolis reconstituido bajo varias condiciones de temperatura y contenedor se muestran en la Tabla 35.
Tabla 35: Estabilidad de Kyprolis Reconstituido
|
Condiciones de Almacenaje de Kyprolis Reconstituido |
Estabilidada por Contenedor |
||
|
Vial |
Jeringa |
Bolsa Intravenosa (D5Wb) |
|
|
Refrigerado (2°C a 8°C; 36°F a 46°F) |
24 horas |
24 horas |
24 horas |
|
Temperatura Ambiente (15°C a 30°C; 59°F a 86°F) |
4 horas |
4 horas |
4 horas |
a Tiempo total desde la reconstitución a la administración no debe exceder 24 horas.
b 5% Dextrosa Inyectable






